Schnelle anwendungsorientierte Analyse robuster in vitro Systeme (SaAr in vitro)
Ziel des Vorhabens und inhaltliche Zusammenfassung:
SaAr in vitro hat das ambitionierte Ziel, entzündliche Erkrankungen des Menschen als Zellmodell abzubilden, um daran im für die Industrie zugänglichen Maßstab neue Arzneimittel und Chemikalien zu testen. Das Projekt basiert auf zwei Schlüsselkomponenten: der anwendungsorientierten massenspektrometrischen Untersuchungsmethode und den humanen zellulären in vitro Modellen. Die Kombination beider Techniken erlaubt es, zielgerichtet neue Arzneimittelformulierungen für den Menschen zu entwickeln und Gefährdungen frühzeitig und ohne Tierversuche zu erkennen. Im Mittelpunkt des Vorhabens stehen entzündliche Erkrankungen des Menschen. Wichtige Adressaten sind Asthma Bronchiale, COPD, Morbus Crohn und die entzündliche Hauterkrankung Psoriasis. Die PharmBioTec greift für das Vorhaben auf jahrelanges eigenes Know-How im Bereich der 3R (Replacement, Reduction & Refinement of animal testing) zurück.
Die sogenannten Omics-Technologien, zu denen auch die im Projekt genutzte Proteomics-Technologie mittels Massenspektrometrie aufbaut, erlaubt es der PharmBioTec gleichzeitig kostengünstig verschiedene Entzündungssignale aus Haut-, Darm-, und Lungenmodellen zu messen. Durch diese Anwendung werden tiefgehende Analysen im hohen Durchsatz zu kostengünstigen Konditionen möglich. Diese Kombination aus menschlichen Zellmodellen und moderner Messtechnik ist in der Anwendung für die chemische und pharmazeutische Industrie günstiger und effizienter als der Einsatz von Tiermodellen und bietet für das Saarland eine neue Chance im Bereich Auftragsforschung.
Ermöglichung des Forschungsprojektes durch Förderung:
Das Projekt SaAr in vitro wird gefördert durch das Programm EFRE Saarland im Ziel „Investitionen in Beschäftigung und Wachstum“ 2021-2027 unter dem Förderkennzeichen EFRE-AuF-0000889. Die Förderperiode erstreckt sich von 01. Mai 2024 bis 31. Juli 2027.



Bisherige Ergebnisse:
I. Proteomic profiling of macrophages: effects of inflammatory activation and anti-inflammatory treatment with IBD therapeutics (Lichtner et al., 2025)
In einer ersten Studie untersuchten wir Veränderungen im Proteom von MDMs (aus menschlichen Monozyten gewonnenen Makrophagen), die zur Modellierung einer Entzündungssituation mit Lipopolysaccharid (LPS) stimuliert wurden. Mittels HPLC‑MS/MS wurden sowohl intra- als auch extrazelluläre Proteinexpressionsmuster analysiert. Die LPS-Stimulation aktivierte zentrale proinflammatorische Signalwege, einschließlich der NF-κB-Signalübertragung, was sich in einer erhöhten Expression von Zytokin- und Adhäsions-bezogenen Proteinen wie IL1B, IL8 und ICAM1 widerspiegelte.
Innerhalb dieses Modells wurden die Wirkmechanismen dreier etablierter IBD‑Therapeutika (Mesalazin, Prednisolon und 6‑Mercaptopurin) systematisch untersucht. Mesalazin bewirkte eine moderate Modulation von Entzündungsregulatoren, während Prednisolon eine deutliche Unterdrückung proinflammatorischer und Komplementproteine auslöste. 6‑Mercaptopurin führte zu umfassenden Veränderungen ribosomaler, metabolischer und apoptoseassoziierter Proteine.
Die Ergebnisse zeigen klare Unterschiede zwischen intra- und extrazellulären Proteinsignaturen und bestätigen die Rolle aktivierter Makrophagen bei der Immunmodulation. Zudem spiegeln die beobachteten proteomischen Veränderungen physiologische Prozesse im menschlichen Körper wider. Insgesamt demonstriert die Studie, dass das LPS‑stimulierte MDM‑Modell wesentliche Aspekte der Makrophagenaktivierung bei IBD abbildet und arzneimittelspezifische proteomische Signaturen liefert. Dies unterstreicht das Potenzial des Assays als prädiktives Modell für menschliche Daten und als Grundlage für personalisierte therapeutische Strategien.
Gesamte Studie hier: Proteomic profiling of macrophages: effects of inflammatory activation and anti-inflammatory treatment with IBD therapeutics – ScienceDirect
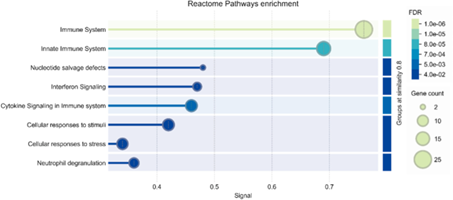
Abbildung 1: Reactome-Pfad-Anreicherungsanalyse von Proteinen aus dem Überstand und dem Lysat von aus Monozyten stammenden Makrophagen, die 24 Stunden lang mit LPS stimuliert wurden (Positivkontrollen), die entweder im Vergleich zu den unstimulierten Negativkontrollen signifikant hochreguliert sind (negativer log10-p-Wert von > 1,3 und ein log2-Verhältnis von ≤ -1 oder ≥1) oder ausschließlich in den LPS-stimulierten Proben gefunden wurden.
Auswahl verschiedener Verwertungen Projekt SaAr in vitro:
- MaxQuant summer school 2024: Poster: „SaAr in vitro: Innovating Drug Testing with Human Co-Culture Cell Models and Mass Spectrometry“
- EUSAAT congress, 2024: Poster: “Investigation of complex in vitro models using shotgun proteomics for the prediction of human-relevant data for
- anti-inflammatory drugs”
- 3R Konferenz Saarbrücken, 2024: Vortrag: “SaAr in vitro – Advancing Drug Safety and Efficacy with in vitro Models and High-Throughput Proteomics in inflammatory diseases”
- HTCR Symposium, 2025: Poster: “Proteomic analyses of human-derived macrophages predict human data for anti-inflammatory drugs”
- MaxQuant summer school, 2025: Poster: “Proteomic analysis of human-derived macrophages and human intestinal cells to predict human responses”
- CRS meets BioBarriers Konferenz 2026: Poster: “SaAr in vitro: Proteomics-Based Cell Culture Models for Predictive Drug Testing in Chronic Inflammation”
- Präsentation des Projekts im Rahmen der Innovationstour des Wirtschaftsministers des Saarlandes, Jürgen Barke (Forschung und Innovation – Innovationstour von Wirtschaftsminister Jürgen Barke – saarland.de)
- Publikation der ersten Studie: Simone Lichtner, Kathrin Schunck, Johanna Frey, Janina Osti, Selina Dannheimer, Sabrina Schnur, Claus-Michael Lehr, Marc Schneider, Marius Hittinger: „Proteomic profiling of macrophages: effects of inflammatory activation and anti-inflammatory treatment with IBD therapeutics“, European Journal of Pharmaceutics and Biopharmaceutics, Volume 216, 2025, https://doi.org/10.1016/j.ejpb.2025.114869.



